Auteurs : Marco Gabutti, Jerry Draper-Rodi
The British School of Osteopathy, London SE1 1JE, UK
Contacts : marco.gabutti chez gmail.com, jerryrodi chez gmail.com
Titre de l’article original : Osteopathic decapitation : why do we consider the head differently from the rest of the body ? New perspectives for an evidence-informed osteopathic approach to the head (International Journal of Osteopathic Medicine, 2014, 17, 256-262) http://dx.doi.org/10.1016/j.ijosm.2014.02.001 Copyright © 2014 Published by Elsevier Ltd. All rights reserved.- Traduction : Marco Gabutti, Jerry Draper-Rodi
Copyright © 2017 SDO-Jean-Louis Boutin pour la traduction française.
Nous remercions les auteurs, Marco Gabutti & Jerry Draper-Rodi d’avoir traduit leur article.
Résumé

L’approche ostéopathique de la tête a été fondée, dès son origine, sur un modèle biomécanique qui se retrouve aujourd’hui largement controversé. La nécessité de concilier la pratique ostéopathique avec les preuves disponibles, ainsi que l’esprit critique que nous attendons de la part de nos étudiants, ne sont plus compatibles avec l’ostéopathie crânienne telle qu’elle a été conçue par Sutherland.
Ces dernières décennies ont vu émerger un nouveau domaine de recherche s’intéressant à la mécanique des tissus vivants. Les ostéopathes pourraient y trouver des éléments utiles à l’élaboration d’un modèle de diagnostic et de traitement de la tête qui serait davantage en adéquation avec l’état actuel des connaissances. La biomécanique ne se limite pas à la cinématique du corps humain. Elle inclut l’étude des propriétés mécaniques des tissus vivants et la manière dont ils se déforment sous l’action des sollicitations extérieures. Ces études ont notamment permis de mieux comprendre le rôle et le développement des sutures crâniennes ainsi que la répartition des contraintes et des déformations sur le crâne.
Bien qu’ils figurent parmi les éléments plus rigides du corps, les os subissent des déformations, tant dans les scènes de la vie quotidienne qu’au cours d’événements traumatiques. Comme pour tout autre matériau, contraintes et déformations naissent au sein du tissu osseux sous l’effet des sollicitations extérieures qui s’y exercent, et les os du crâne ne constituent pas une exception.
Dans cet article nous passons en revue les propriétés mécaniques des os et des sutures du crâne et mettons en évidence le rôle primordial que jouent les muscles dans les déformations du crâne. L’action des muscles qui se contractent est désormais reconnue comme l’une des principales causes de sollicitation du tissu osseux : en dehors des événements traumatiques, un nombre conséquent de publications sur le comportement mécanique des os et sutures du crâne confirme le rôle prépondérant que jouent les muscles dans les déformations de la tête.
Mots-clés : ostéopathie crânienne ; tête ; mécanique des tissus vivants ; déformations crâniennes ; muscles masticateurs
Introduction
L’approche ostéopathique de la tête a été initialement fondée sur un modèle biomécanique (1) qui demeure largement controversé (2-4). La nécessité de concilier la pratique de l’ostéopathie avec les preuves disponibles, ainsi que l’esprit critique que nous attendons de nos étudiants, ne sont plus compatibles avec le modèle d’ostéopathie crânienne tel qu’il a été élaboré par Sutherland.
Bien que les questions relatives aux fondements physiologiques et à l’efficacité clinique de l’ostéopathie crânienne (OC) mériteraient une attention particulière (2), leur analyse dépasse le cadre de cet article. Les principales recherches consacrées à l’OC ont été menés dans l’idée de prouver la validité des intuitions de Sutherland, de confirmer le bien-fondé de la pratique de l’ostéopathie crânienne (6-9) en tant que telle et de convaincre la communauté scientifique de la pertinence des concepts sous-tendant la pratique de l’OC.
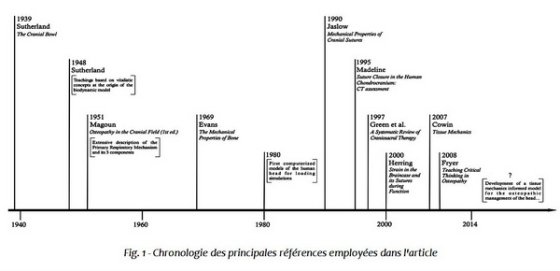
Nous souhaitons, à travers cet article, attirer l’attention des enseignants et des étudiants sur l’état des connaissances dans le domaine des propriétés mécaniques du crâne. Ces travaux présentent l’avantage d’être largement admis et partagés au sein de la communauté scientifique, mais ils représentent aussi pour notre profession autant d’occasions de revoir et affiner le modèle explicatif employé dans l’approche ostéopathique de la tête en général (Fig. 1).
Cet article s’inscrit dans une démarche déductive, en commençant par collecter et analyser les meilleures preuves disponibles au sujet des propriétés mécaniques de la tête, c’est-à-dire du crâne et ses tissus environnants. Nous espérons fournir des données fiables et récentes pouvant servir de base aux développements à venir concernant les approches ostéopathiques de la tête, tant en matière de palpation que de critères diagnostiques et de techniques de traitement. Les différentes approches devront être ensuite évaluées cliniquement afin d’en déterminer la validité.
De la biomécanique à la mécanique des tissus : un changement de paradigme
L’OC étant née dans les années 1930 il n’est pas surprenant de la voir décrite en termes biomécaniques (1-10). La biomécanique est parfaitement adaptée à l’étude des moments et forces donnant naissance aux mouvements des différents segments osseux et articulations au cours des gestes quotidiens. Sutherland a construit son modèle d’après une étude minutieuse réalisée sur des crânes secs11. Bien que la démarche consistant à déduire le mouvement relatif des os du crâne en étudiant la forme des sutures soit tout à fait pertinente, comme cela a été confirmé dans des études animales (12-14), les hypothèses de Sutherland quant à une motilité inhérente du système nerveux central, et qui serait à l’origine des déformations crâniennes, est incompatible avec les connaissances actuelles (3,15). En ce sens, les polémiques autour du modèle crânien sont largement justifiées. Certains ostéopathes ont surmonté l’insatisfaction liée au modèle biomécanique en le substituant par une approche plus subtile, énergétique ou fluidique (16), mais l’absence de preuves demeure un obstacle majeur à son enseignement dans les écoles ainsi qu’à une stratégie de recherche pluridisciplinaire.
Entretemps, l’étude des propriétés mécaniques des tissus vivants a continuellement progressé jusqu’à devenir un domaine de recherche à part entière (17), fournissant une quantité considérable de données susceptibles d’intéresser tout ostéopathe cherchant à élaborer des modèles explicatifs cohérents et conformes aux connaissances actuelles.
La biomécanique est souvent considérée à tort comme la seule application de la cinématique au corps humain. Elle inclut également l’étude du comportement mécanique des tissus vivants : la manière dont ils se déforment, résistent ou cèdent, sous l’action des sollicitations les plus variées. Ce sous-domaine de la biomécanique permet de mieux comprendre des phénomènes aussi divers que les déformations du tibia au cours de la marche, de la course ou du saut18, les mécanismes sous-tendant le phénomène de fracture de fatigue (19-21), la dégénérescence des disques intervertébraux(22,23) ainsi que les procédés complexes de micro-fracture et de remodelage osseux (24,25). L’étude du comportement mécanique des tissus vivants permet de mieux comprendre comment les tissus se déforment lorsqu’ils sont sollicités (17,26). Elle a notamment permis d’explorer plus précisément le rôle et le développement des sutures crâniennes ainsi que la répartition des contraintes et déformations sur les crânes de plusieurs espèces de primates. (27-31)
Cet article est destiné à dresser une synthèse de ces découvertes afin de les rendre accessibles aux étudiants et aux enseignants en ostéopathie.
Quelques notions fondamentales en mécanique des tissus vivants
Lorsqu’une force est appliquée à un objet sans que celui-ci puisse se mouvoir, tant en translation qu’en rotation, cet objet se déforme. La sollicitation d’un matériau génère en son sein des contraintes (stresses en anglais). Il y a deux sortes de contraintes : les contraintes normales, notées sigma (σ), qui tendent à écarter ou comprimer les particules les unes des autres, et les contraintes tangentielles, ou de cisaillement, notées tau (τ), qui tendent à faire glisser les particules les unes sur les autres. Les contraintes sont exprimées en N/m2 (Pa) et rendent compte de la manière dont la sollicitation extérieure se répartit au sein de l’objet sollicité. Lorsqu’un objet se déforme, on note epsilon (ε) la proportion dans laquelle il change de taille. Cette dilatation (ε), ou contraction, (strain en anglais) est exprimée en pourcentage de la longueur initiale : ε est positif si l’objet s’allonge, négatif s’il se raccourcit. Lorsque les déformations sont particulièrement faibles, comme c’est le cas pour le tissu osseux, elles sont exprimées en millionième de la longueur initiale. On retrouve régulièrement dans la littérature les déformations exprimées en microstrain (με). 1 με correspond à une déformation de 0,00001 %.
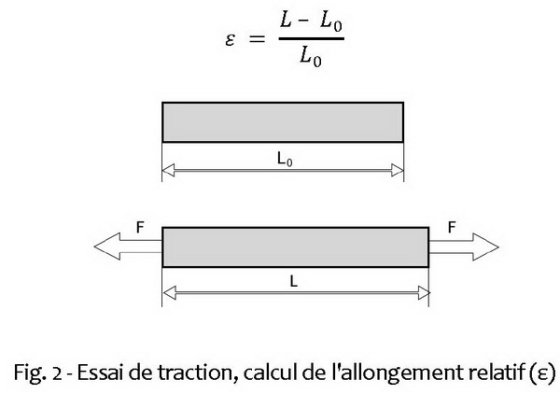
Contraintes et déformations ne sont pas indépendantes. Il est assez simple de se représenter que plus on sollicite un objet, plus il va se déformer et plus les contraintes en son sein vont être importantes. Dans certains cas les contraintes sont proportionnelles à l’allongement, la relation entre contraintes et déformation est alors linéaire et leur relation peut s’écrire sous la forme :
σ = E x ε
E est appelé module d’élasticité, exprimé en N/m2 (Pa).
Contrairement à ce qu’il laisse penser de prime abord, le module d’élasticité ne reflète pas une éventuelle souplesse du matériau mais plutôt sa raideur. Pour donner un ordre de grandeur, le module d’élasticité E du tissu osseux cortical avoisine les 15000 MPa,32,33 alors que celui de tissus plus souples comme les sutures crâniennes tourne autour de 50 MPa. (34)
Les os du crâne
Propriétés mécaniques du tissu osseux
L’étude du comportement mécanique du tissu osseux et des os a toujours posé de nombreuses difficultés, tant pour biologistes que pour les spécialistes en mécanique des matériaux (35). Lors des premières recherches dans le domaine, comme l’illustre bien l’article d’Evans (1969) (36), les os étaient réduits à un simple rôle de poutre ou de colonne. On a découvert depuis que les propriétés mécaniques des os étaient bien plus variées et complexes qu’initialement présumé (17,37).
Le tissu osseux présente quelques particularités essentielles à la compréhension de son comportement (42) :
1. L’os ne se déforme pas proportionnellement aux efforts qu’il supporte. La relation contrainte/déformation n’est pas linéaire. Son comportement mécanique peut même varier suivant le rythme auquel on le sollicite (38,40,41). A ce titre, l’os se comporterait davantage comme un matériau visco-élastique (38,39). Certains auteurs ont même poussé la modélisation jusqu’à prendre en compte le rôle des fluides contenus dans l’os vivant, et ont décrit le comportement poro-élastique du tissus osseux (1).7
2. L’os est un matériau composite hétérogène, constitué de différents types de tissus osseux, chacun d’eux possédant des propriétés mécaniques différentes (39,42 ).
3. L’os est un matériau anisotrope, ses propriétés mécaniques ne sont pas identiques suivant qu’on le sollicite dans une direction ou une autre (32,38,43).
4. L’os est un matériau vivant, en renouvellement constant, capable de se réparer et présentant des propriétés mécaniques différentes dans chaque période la vie.24,44,45
Bien qu’il figure parmi les matériaux les plus durs et rigides du corps, l’os n’en subit pas moins des déformations durant les activités de la vie courante et, a fortiori, les évènements traumatiques. Le tissu osseux est sujet à contraintes et déformations comme tout autre matériau (18,42-44,46-48), et les os du crâne ne font pas exception (12,31,33,41,49).
Propriétés mécaniques des os du crâne
Les tentatives de détermination des propriétés mécaniques des os du crâne ont débuté dans les années 1960. Leur but initial était de comprendre et prévenir les traumatismes crâniens mais également de construire des modèles suffisamment fidèles pour pouvoir simuler différents types d’impacts et sollicitations (36,50,51).
Les recherches concernant les propriétés mécaniques des os du crâne peuvent être menées globalement de deux façons. La première consiste à prélever des échantillons de tissu osseux sur des cadavres et de soumettre ces échantillons à des tests de déformation et résistance (50,52). La deuxième méthode consiste à mesurer les déformations directement sur le crâne de sujets vivants. Ce procédé est plus à même d’intéresser les thérapeutes manuels car il permet de savoir comment l’ensemble du crâne réagit aux sollicitations, que ce soit dans des situations courantes comme durant la mastication, ou lors de chocs, voire lors d’un traitement manuel.
Les mesures in-vivo, principalement obtenues sur des mini-porcs (de l’espèce sus scrofa) et des primates, montrent que le crâne se déforme sous l’effet de la mastication, que les sutures soient soudées ou non (12,28) Les déformations mesurées sur le frontal et le pariétal des mini-porcs durant la mastication avoisine les 50 με (0,0005%), ce qui représente un allongement ou raccourcissement d’environ 2,5 μm. Les chercheurs ont établi que l’agencement et les tailles relatives des muscles masticateurs ainsi que l’ordre de grandeur des forces de mastication sont comparables chez les mini-porcs et les primates (12,34,49), et que la géométrie et la structure du crâne, de la mandibule et des muscles cervicaux des primates sont plus proches de celles de l’humain que des autres mammifères (37). Par conséquent, bien que les valeurs obtenues lors des expérimentations sur des mini-porcs diffèrent de celles qui auraient été obtenues sur des sujets humains, l’ordre de grandeur serait très probablement semblable. Currey cite une expérience que Hillam a conduite sur lui-même lors de la réalisation de sa thèse sur les réponses du tissu osseux aux sollicitations mécaniques (42). Hillam a installé des capteurs sur son propre crâne et a enregistré des déformations autour de 100 à 200 με durant des activités courantes comme la mastication, le rire ou taper dans une balle avec sa tête. Ces résultats viennent renforcer la pertinence des analogies, en termes d’ordre de grandeur, des résultats obtenus chez les mini-porcs, les primates et les humains.
Les sutures crâniennes
On reconnaît aux sutures deux rôles principaux : permettre la croissance osseuse du crâne et améliorer l’aptitude de la tête à absorber l’énergie des impacts (34,53,54).
Âge de fermeture des sutures
Les sutures jouent un rôle primordial dans la croissance osseuse. La manière et l’âge auquel les sutures se soudent dépendent de leur de leur appartenance ou non au chondrocrâne.
Les sutures du chondrocrâne
Les sutures de la base du crâne fusionnent progressivement durant l’enfance et l’adolescence et sont totalement absentes une fois la croissance terminée. L’étude conduite par Madeline55 fournit des données exhaustives sur le sujet des sutures de la base du crâne et de leur âge de fusion respectifs. D’autres recherches sont venues par la suite confirmer les résultats de Madeline (56,57). Les ostéopathes ne peuvent légitimement pas continuer à ignorer ces données et devraient au moins réserver les modèles explicatifs supposant la présence de sutures dans le chondrocrâne à la prise en charge des enfants et adolescents.
Les sutures de la face et de la voûte
L’évolution des sutures de la voûte et de la face est sensiblement différente de celle de la base du crâne. La littérature, essentiellement issue de la médecine légale, reporte de nombreux cas de sutures non soudées au niveau de la voûte chez les adultes, même au-delà de l’âge de 50 ans (58). De nombreuses recherches ont été consacrées à la fiabilité de l’estimation de l’âge des cadavres adultes par l’analyse du degré de fermeture des sutures de la voûte (58,59).
Propriétés mécaniques des sutures du crâne
Les propriétés mécaniques des sutures du crâne ont été largement explorées chez de nombreuses espèces au cours des trente dernières années (12,53,60,61). Les principales informations qu’on peut en retenir sont les suivantes :
1. Les sutures jouent un rôle indispensable dans la croissance osseuse du crâne (12,62 ).
2. La mastication entraîne alternativement des contraintes de traction et de compression au sein des sutures, notamment par l’intermédiaire des muscles masticateurs qui s’y insèrent. Le phénomène qui s’ensuit, baptisé mécanotransduction, est responsable de l’activation des cellules contenues dans les sutures et contribue au développement normal des os du crâne (62,63).
3. Les sutures améliorent considérablement les capacités du crâne à absorber les chocs, notamment grâce à leur plus grande souplesse comparée au tissu osseux (34,54). A contrainte égale, les sutures crâniennes se déforment 10 fois plus (env. 500 με) que les os adjacents (50 με) (12 ).
4. La manière et la mesure dans laquelle les sutures modifieraient la répartition des contraintes sur le crâne reste l’objet de discussions. Les dernières recherches tendent à montrer que les sutures jouent un rôle négligeable sur la distribution globale des contraintes et déformation sur le crâne, mais elles pourraient jouer un rôle sur la distribution locale de ces mêmes contraintes et déformations (27,34).
Les mouvements supposés des os dans le modèle de Sutherland reposent sur la présence de sutures cartilagineuses mais, comme nous venons de le voir, cette condition n’est pas présente tout au long de la vie d’un individu. La fermeture des sutures est un processus particulièrement complexe et progressif, des spicules osseux peuvent constituer un pont bien avant que la suture soit complètement soudée (55). Par conséquent, tout modèle reposant sur la présence de sutures devrait être au moins limité à la période de vie précédent les premières étapes de fusion. Les futurs modèles explicatifs devraient prendre en compte les propriétés mécaniques des sutures mais également la période intermédiaire, en cours de fusion, et la période suivant la fermeture complète.
Les muscles crâniens
L’action des muscles sur les os sur lesquels ils s’insèrent, et les réactions qui s’ensuivent, est maintenant reconnus comme la source principale de sollicitation du tissus osseux (42,44,64,65), et encore une fois la tête n’y échappe pas. Une abondante littérature au sujet des propriétés mécaniques du crâne vient confirmer le rôle primordial que jouent les muscles dans les déformations du crâne (14,30,49,60,65,66).
Les muscles sont pratiquement absents du modèle crânien de Sutherland. Ce qui pourrait être justifié par son étude basée presque exclusivement sur crânes secs, pratique courante à cette époque. Il a par ailleurs émis l’hypothèse suivant laquelle le crâne se déformerait sous l’action de la motilité inhérente du système nerveux central et/ou d’une fluctuation du liquide céphalo-rachidien. En parallèle, des travaux remarquables permettant de mieux comprendre la répartition des contraintes au sein de la tête et les déformations du crâne ont été menés durant plus de quarante ans sans qu’il ait été nécessaire de recourir aux hypothèses avancées par Sutherland et une partie de ses successeurs.
Les futurs modèles explicatifs en ostéopathie crânienne devraient au moins prendre en compte toutes les structures réputées importantes dans la transmission des efforts et des déformations subies par la tête, tant lors des actions de la vie quotidienne que durant les chocs.
Conclusion
Les données actuellement disponibles dans le domaine de la mécanique des tissus vivants constituent une source importante de preuves permettant de revisiter les modèles explicatifs employés pour expliquer l’approche ostéopathie de la tête. Ces données devraient au moins amener les ostéopathes à reconsidérer la pertinence d’un modèle spécifique pour le diagnostic et le traitement de la tête, adopter un même modèle qui serait applicable à l’ensemble du corps serait probablement préférable et davantage cohérent.
Les points-clés de ce commentaire sont les suivants :
1. Les os du crâne se déforment durant les actions de la vie quotidienne et plus encore durant les chocs.
2. Les muscles de la tête constituent la principale cause de déformations du crâne
3. Les sutures peuvent affecter la manière dont la tête se déforme, mais la tête se déforme même en l’absence de sutures.
Références
1. Sutherland W. The cranial bowl : A treatise relating to cranial articular mobility, cranial articular lesions and cranial techniques. (Co FP, ed.). Mankato ; 1939.
2. Green C, Martin CW, Bassett K, Kazanjian A. A systematic review of craniosacral therapy : biological plausibility, assessment reliability and clinical effectiveness. Complement Ther Med. 1999 ;7(4):201–207. https://www.iahe.com/images/pdf/SystematicReview.pdf
3. Hartman SE. Cranial osteopathy : its fate seems clear. Chiropr Osteopat. 2006 ;14:10. doi:10.1186/1746-1340-14-10. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC1564028/ [en ligne] - Voir sur le SDO la traduction de cet article : Ostéopathie crânienne : Son destin semble évident
4. Ernst E. Craniosacral therapy : a systematic review of the clinical evidence. Focus on Alternative and Complementary Therapies. 2012. http://onlinelibrary.wiley.com/doi/10.1111/j.2042-7166.2012.01174.x/abstract
5. Fryer G. Teaching critical thinking in osteopathy – Integrating craft knowledge and evidence-informed approaches. International Journal of Osteopathic Medicine. 2008 ;11(2):56–61. http://dx.doi.org/10.1016/j.ijosm.2008.02.005
6. Cook A. The SBS Revisited-The Mechanics of Cranial Motion. Journal of Bodywork and Movement Therapies. 2005 ;9(3):177–188. http://www.hummingbird-one.co.uk/pdf/sbs_JBMT.pdf [en ligne]
7. Hamm D. A hypothesis to explain the palpatory experience and therapeutic claims in the practice of osteopathy in the cranial field. International Journal of Osteopathic Medicine. 2011 ;14(4):149–165. http://dx.doi.org/10.1016/j.ijosm.2011.07.003
8. Seimetz CN, Kemper AR, Duma SM. An investigation of cranial motion through a review of biomechanically based skull deformation literature. International Journal of Osteopathic Medicine. 2012 ;15(4):152–165. DOI : http://dx.doi.org/10.1016/j.ijosm.2013.07.007
9. Sergueef N, Greer MA, Nelson KE, Glonek T. The palpated cranial rhythmic impulse (CRI) : Its normative rate and examiner experience. International Journal of Osteopathic Medicine. 2011 ;14(1):10–16. http://doi.org/10.1016/j.ijosm.2010.11.006
10. Magoun H. Osteopathy in the Cranial Field. (published S, ed.). Denver : Self Published ; 1951.
11. Sutherland AS. With Thinking Fingers. The Cranial Academy ; 1962.
12. Herring SW, Teng S. Strain in the braincase and its sutures during function. Am J Phys Anthropol. 2000 ;112(4):575–593. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC2813197/ [en ligne]
13. Markey MJ, Marshall CR. Linking form and function of the fibrous joints in the skull : A new quantification scheme for cranial sutures using the extant fishPolypterus endlicherii. J Morphol. 2006 ;268(1):89–102. http://onlinelibrary.wiley.com/doi/10.1002/jmor.10504/full
14. Ross CF. Does the Primate Face Torque ? Primate Craniofacial Function and Biology. 2008:63–81.
15. Downey PA, Barbano T, Kapur-Wadhwa R, Sciote JJ, Siegel MI, Mooney MP. Craniosacral therapy : the effects of cranial manipulation on intracranial pressure and cranial bone movement. J Orthop Sports Phys Ther. 2006 ;36(11):845–853. https://www.iahe.com/images/pdf/2451_001.pdf [en ligne]
16. McPartland JM, Skinner E. The biodynamic model of osteopathy in the cranial field. Explore : The Journal of Science and Healing. 2005 ;1(1):21–32. http://www.explorejournal.com/article/S1550-8307(04)00006-0/abstract [Voir également : John M McPartland and Evelyn Skinner : The biodynamic model of osteopathy in the cranial field - Chapter 4, http://leonchaitow.com/wp-content/uploads/cranialpdfs/Ch04.pdf en ligne]
17. Cowin SC, Doty SB. Tissue Mechanics. New York, NY : Springer ; 2007.
18. Yang PF, Brüggemann G-P, Rittweger J. What do we currently know from in vivo bone strain measurements in humans ? J Musculoskelet Neuronal Interact. 2011 ;11(1):8–20. http://www.ismni.org/jmni/pdf/43/02YANG.pdf
19. Devulder A, Aubry D, Puel G. Two-time scale fatigue modelling : application to damage. Comput Mech. 2010 ;45(6):637–646. https://hal.archives-ouvertes.fr/hal-00707975/document [en ligne]
20. Frost HM. New targets for fascial, ligament and tendon research : a perspective from the Utah paradigm of skeletal physiology. J Musculoskelet Neuronal Interact. 2003 ;3(3):201–209. http://www.ismni.org/jmni/pdf/13/03FROST.pdf. [en ligne]
21. Turner CH. Bone strength : current concepts. Ann N Y Acad Sci. 2006 ;1068:429–446. https://www.fields.utoronto.ca/programs/scientific/08-09/biomedical/proposed_problems/Turner_bone_strength.pdf [en ligne]
22. Adams MA, Stefanakis M, Dolan P. Healing of a painful intervertebral disc should not be confused with reversing disc degeneration : Implications for physical therapies for discogenic back pain. Clinical Biomechanics. 2010 ;25(10):961–971. http://doi.org/10.1016/j.clinbiomech.2010.07.016
23. Adams MA. Biomechanics of back pain. Acupunct Med. 2004 ;22(4):178–188. http://aim.bmj.com/content/22/4/178.long
24. Doblaré M, García J, Gómez M. Modelling bone tissue fracture and healing : a review. Engineering Fracture Mechanics. 2004 ;71(13-14):1809–1840. http://doi.org/10.1016/j.engfracmech.2003.08.003
25. Mulvihill BM, Prendergast PJ. Mechanobiological regulation of the remodelling cycle in trabecular bone and possible biomechanical pathways for osteoporosis. Clin Biomech (Bristol, Avon). 2010 ;25(5):491–498. http://doi.org/10.1016/j.clinbiomech.2010.01.006
26. Mikos AG, Herring SW, Ochareon P, et al. Engineering Complex Tissues. Tissue Engineering. 2006 ;12(12):3307–3339. http://orion.bme.columbia.edu/lulab/pdf/Mikos_Engineering-Complex-Tissue_2006.pdf [en ligne]
27. Wang Q, Wood SA, Grosse IR, et al. The role of the sutures in biomechanical dynamic simulation of a macaque cranial finite element model : implications for the evolution of craniofacial form. Anat Rec (Hoboken). 2012 ;295(2):278–288. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3365596/ [en ligne]
28. Ross CF, Berthaume MA, Dechow PC, et al. In vivo bone strain and finite-element modeling of the craniofacial haft in catarrhine primates. J Anat. 2011 ;218(1):112–141. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3039785/pdf/joa0218-0112.pdf [en ligne]
29. Wood SA, Strait DS, Dumont ER, Ross CF, Grosse IR. The effects of modeling simplifications on craniofacial finite element models : the alveoli (tooth sockets) and periodontal ligaments. Journal of Biomechanics. 2011 ;44(10):1831–1838. https://doi.org/10.1016/j.jbiomech.2011.03.022
30. Chalk J, Richmond BG, Ross CF, et al. A finite element analysis of masticatory stress hypotheses. Am J Phys Anthropol. 2011 ;145(1):1–10. http://onlinelibrary.wiley.com/doi/10.1002/ajpa.21416/abstract
31. Strait DS, Wang Q, Dechow PC, et al. Modeling elastic properties in finite-element analysis : How much precision is needed to produce an accurate model ? Anat Rec. 2005 ;283A(2):275–287. http://onlinelibrary.wiley.com/doi/10.1002/ar.a.20172/full [en ligne]
32. Wirtz DC, Schiffers N, Pandorf T, Radermacher K, Weichert D, Forst R. Critical evaluation of known bone material properties to realize anisotropic FE-simulation of the proximal femur. Journal of Biomechanics. 2000 ;33(10):1325–1330. http://web.mit.edu/awinter/Public/MGH%20Literature/Wirtz-2000-Evaluation%20of%20known%20bone%20material%20properties.pdf [en ligne]
33. Belingardi G, Chiandussi G, Gaviglio I. Development and validation of a new finite element model of human head. Proceedings 19th ESV (Enhanced Safety on Vehicles). 2005. https://pdfs.semanticscholar.org/43db/aa34cb3d3796de52faf896ed58a04f081990.pdf [en ligne]
34. Wang Q, Smith AL, Strait DS, et al. The Global Impact of Sutures Assessed in a Finite Element Model of a Macaque Cranium. Anat Rec. 2010 ;293(9):1477–1491. http://onlinelibrary.wiley.com/doi/10.1002/ar.21203/full [en ligne]
35. Currey J. Measurement of the mechanical properties of bone : a recent history. Clin Orthop Relat Res. 2009 ;467(8):1948–1954. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC2706353/ [en ligne]
36. Evans FG. The mechanical properties of bone. Artif Limbs. 1969 ;13(1):37–48.
37. Yue X, Wang L, Zhou F. Finite element analysis on strains of viscoelastic human skull and duramater. Journal of Basic Science and Engineering 2008 ;16(5):686–694. https://www.intechopen.com/books/finite-element-analysis/finite-element-analysis-on-strains-of-viscoelastic-human-skull-and-duramater [en ligne]
38. Iyo T, Maki Y, Sasaki N, Nakata M. Anisotropic viscoelastic properties of cortical bone. Journal of Biomechanics. 2004 ;37(9):1433–1437. http://www.umich.edu/~bme332/ch9bone/viscoelasticbone.pdf [en ligne]
39. Sasaki N. Viscoelastic Properties of Biological Materials. In : De Vicente J, ed. Viscoelasticity - From Theory to Biological Applications. InTech ; 2012:99–122. https://www.intechopen.com/books/viscoelasticity-from-theory-to-biological-applications/viscoelastic-properties-of-biological-materials [en ligne]
40. Hansen U, Zioupos P, Simpson R, Currey JD, Hynd D. The effect of strain rate on the mechanical properties of human cortical bone. J Biomech Eng. 2008 ;130(1):011011. http://biomechanical.asmedigitalcollection.asme.org/article.aspx?articleid=1475452
41. Motherway JA, Verschueren P, Van der Perre G, Vander Sloten J, Gilchrist MD. The mechanical properties of cranial bone : the effect of loading rate and cranial sampling position. Journal of Biomechanics. 2009 ;42(13):2129–2135. http://dx.doi.org/10.1016/j.jbiomech.2009.05.030 Voir également : http://www.ircobi.org/wordpress/downloads/irc0111/2010/Session2/2-4.pdf [en ligne]
42. Currey JD. Bones : structure and mechanics. Pinceton, NJ : Princeton Univ Pr ; 2002.
43. Rho J-Y, Kuhn-Spearing L, Zioupos P. Mechanical properties and the hierarchical structure of bone. Med Eng Phys. 1998 ;20(2):92–102. http://www.sciencedirect.com/science/article/pii/S1350453398000071
44. Burr DB. Muscle strength, bone mass, and age-related bone loss. J Bone Miner Res. 1997 ;12(10):1547–1551. http://onlinelibrary.wiley.com/doi/10.1359/jbmr.1997.12.10.1547/full [en ligne]
45. Frost HM. Cybernetic aspects of bone modeling and remodeling, with special reference to osteoporosis and whole-bone strength. Am J Hum Biol. 2001 ;13(2):235–248. http://onlinelibrary.wiley.com/doi/10.1002/1520-6300(200102/03)13:2%3C235::AID-AJHB1034%3E3.0.CO ;2-M/abstract
46. Burr DB. Why bones bend but don’t break. J Musculoskelet Neuronal Interact. 2011 ;11(4):270–285. https://scholarworks.iupui.edu/bitstream/handle/1805/4620/Burr-2011-why.pdf [en ligne]
47. Frost HM. Why should many skeletal scientists and clinicians learn the Utah paradigm of skeletal physiology ? J Musculoskelet Neuronal Interact. 2001 ;2(2):121–130. http://www.ismni.org/jmni/pdf/6/frost1.pdf. [en ligne]
48. de Jong WC, Koolstra JH, Korfage JAM, van Ruijven LJ, Langenbach GEJ. The daily habitual in vivo strain history of a non-weight-bearing bone. Bone. 2010 ;46(1):196–202 http://www.thebonejournal.com/article/S8756-3282(09)01994-2/abstract
49. Herring SW, Rafferty KL, Liu ZJ, Marshall CD. Jaw muscles and the skull in mammals : the biomechanics of mastication. Comp Biochem Physiol, Part A Mol Integr Physiol. 2001 ;131(1):207–219. http://citeseerx.ist.psu.edu/viewdoc/download?doi=10.1.1.319.4285&rep=rep1&type=pdf [en ligne]
50. McElhaney JH, Fogle JL, Melvin JW, Haynes RR, Roberts VL, Alem NM. Mechanical properties of cranial bone. Journal of Biomechanics. 1970 ;3(5):495–511. https://doi.org/10.1016/0021-9290(70)90059-X
51. Wood JL. Dynamic response of human cranial bone. Journal of Biomechanics. 1971 ;4(1):1–12. http://www.sciencedirect.com/science/article/pii/002192907090059X
52. Robbins D, Wood J. Determination of mechanical properties of the bones of the skull. Experimental Mechanics. 1969 ;9(5):236–240. http://link.springer.com/article/10.1007/BF02326542
53. Jaslow CR. Mechanical properties of cranial sutures. Journal of Biomechanics. 1990 ;23(4):313–321. https://www.ncbi.nlm.nih.gov/pubmed/2335529
54. Coats B, Margulies SS. Material properties of human infant skull and suture at high rates. J Neurotrauma. 2006 ;23(8):1222–1232. https://www.seas.upenn.edu/~injury/Publications/Coats_Margulies_2006.pdf [en ligne]
55. Madeline LA, Elster AD. Suture closure in the human chondrocranium : CT assessment. Radiology. 1995 ;196(3):747–756. http://pubs.rsna.org/doi/pdf/10.1148/radiology.196.3.7644639
56. Shirley NR, Jantz RL. Spheno-occipital synchondrosis fusion in modern Americans. J Forensic Sci. 2011 ;56(3):580–585. http://onlinelibrary.wiley.com/wol1/doi/10.1111/j.1556-4029.2011.01705.x/abstract
57. Bassed RB, Briggs C, Drummer OH. Analysis of time of closure of the spheno-occipital synchondrosis using computed tomography. Forensic Sci Int. 2010 ;200(1-3):161–164. http://www.fsijournal.org/article/S0379-0738(10)00181-7/abstract
58. Galera V, Ubelaker DH, Hayek LA. Comparison of macroscopic cranial methods of age estimation applied to skeletons from the Terry Collection. J Forensic Sci. 1998 ;43(5):933–939. https://www.ncbi.nlm.nih.gov/pubmed/9729807
59. Harth S, Obert M, Ramsthaler F, Reuss C, Traupe H, Verhoff MA. Ossification degrees of cranial sutures determined with flat-panel computed tomography : narrowing the age estimate with extrema. J Forensic Sci. 2010 ;55(3):690–694. http://onlinelibrary.wiley.com/doi/10.1111/j.1556-4029.2010.01342.x/abstract
61. Rice D. Craniofacial Sutures - Development, Disease and Treatment. Basel : Karger ; 2008. https://www.karger.com/Book/Home/233650
61. Herring SW, Mucci RJ. In vivo strain in cranial sutures : The zygomatic arch. J Morphol. 1991 ;207(3):225–239. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC2814820/pdf/nihms171104.pdf [en ligne]
62. Sun Z, Lee E, Herring SW. Cranial sutures and bones : Growth and fusion in relation to masticatory strain. Anat Rec. 2004 ;276A(2):150–161. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC2813868/pdf/nihms171168.pdf [en ligne]
63. Mao JJ. Mechanobiology of Craniofacial Sutures. Journal of Dental Research. 2002 ;81(12):810–816. http://journals.sagepub.com/doi/pdf/10.1177/154405910208101203
64. Schönau E, Werhahn E, Schiedermaier U, et al. Influence of muscle strength on bone strength during childhood and adolescence. Horm Res. 1996 ;45 Suppl 1:63–66. https://www.karger.com/Article/PDF/184834
65. de Jong WC, Korfage JAM, Langenbach GEJ. The role of masticatory muscles in the continuous loading of the mandible. J Anat. 2011 ;218(6):625–636. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3125896/pdf/joa0218-0625.pdf [en ligne]
66. Behrents RG, Carlson DS, Abdelnour T. In Vivo Analysis of Bone Strain about the Sagittal Suture in Macaca mulatta during Masticatory Movements. Journal of Dental Research. 1978 ;57(9):904–908. https://deepblue.lib.umich.edu/bitstream/handle/2027.42/67398/10.1177_00220345780570091401.pdf [en ligne]